- การใช้ประโยชน์ของไคโตแซนในการยืดอายุของอาหารและเครื่องดื่ม
- คำนิยามและองค์ประกอบของไคโตแซน (Definition and composition of chitosan)
- ลักษณะเฉพาะของไคโตแซน (Characteristics of chitosan)
- แหล่งวัตถุดิบในธรรมชาติของไคตินและไคโตแซน (Nature source of chitin and chitosan)
- การผลิตไคตินและไคโตแซน (Production of chitin and chitosan)
- ประโยชน์ของไคโตแซนในการยืดอายุอาหารและเครื่องดื่ม
- บทสรุป
- อ้างอิง
- All Pages
Page 5 of 8
การผลิตไคตินและไคโตแซน (Production of chitin and chitosan)
ไคตินและไคโตแซนเป็นสารพอลิแซ็กคาไรด์ที่ผลิตได้จากแหล่งต่างๆ เช่น สัตว์จำพวกกุ้งและปู (crustacean) หอย (mollusks) แมลง สาหร่าย พวกเห็ดราและยีสต์ (รูปที่ 2) ในปัจจุบันแหล่งผลิตไคตินและ ไคโตแซนที่สำคัญคือ เปลือกแข็งของสัตว์จำพวกกุ้งและปู (Synowiecki, J. and Al-Khateeb, NA., 2003) โดยมีกระบวนการผลิตดังนี้
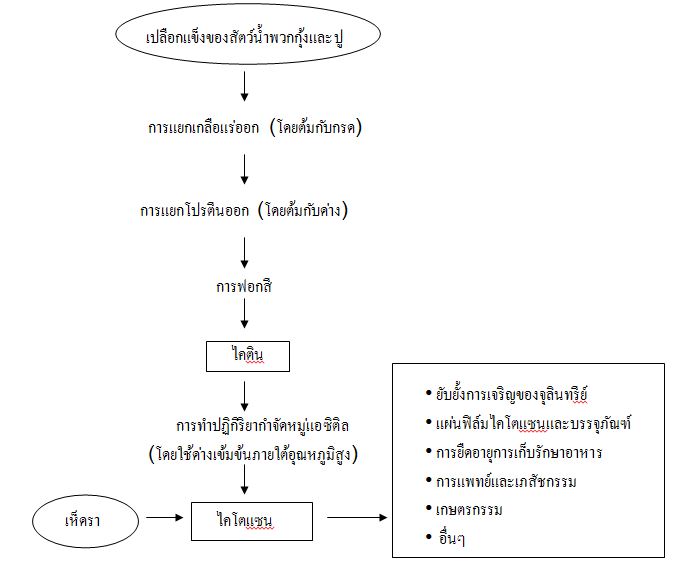
รูปที่ 2 กระบวนการผลิตไคตินและไคโตแซน
1.การผลิตไคติน ประกอบด้วยกระบวนการกำจัดเกลือแร่ (demineralization) กระบวนการกำจัดโปรตีน (deproteinization) และกระบวนการกำจัดหรือฟอกสี (decolourization หรือ bleaching) ซึ่ง 2 กระบวนการแรกสามารถสลับลำดับการทำก่อนหรือหลังได้ ขึ้นอยู่กับการนำไคตินไปใช้ประโยชน์และวิธีการแยกโปรตีนและสารคาโรทีนอยด์ (carotenoids and protein recovery) โดยกระบวนการผลิตไคตินมีรายละเอียดดังนี้
A. กระบวนการกำจัดเกลือแร่ (Demineralization) เป็นขั้นตอนการสกัดเปลือกแข็งโดยการนำวัตถุดิบมาทำปฏิกิริยากับกรดซึ่งโดยทั่วไปใช้กรดไฮโดรคลอริก (hydrochloric acid) เจือจาง (1-8 %) เป็นเวลา 1-3 ชั่วโมงที่อุณหภูมิห้อง นอกจากนี้สามารถใช้กรดฟอร์มิก (formic acid, 90%), กรดไฮโดรคลอริก (ที่ความเข้มข้น 22%, 37%, หรือ 6N ) กรดอะซิติก (acetic acid) หรือ กรดซัลฟูริกหรือกรดกำมะถัน (sulfuric acid) ในสภาวะต่างๆ ที่เหมาะสมทำให้เกลือแร่ถูกกำจัดออกไป การกำจัดเกลือแร่จะทำได้สมบูรณ์เมื่อปริมาณของกรดสูงกว่าเกลือแร่ การทำปฏิกิริยาเป็นเวลานาน (ถึง 24 ชั่วโมง) ทำให้ไคตินแตกสลายได้
B. กระบวนการกำจัดโปรตีน (Deproteinization) เป็นขั้นตอนการแยกโปรตีนออก โดยการทำปฏิกิริยากับด่าง เช่น สารละลายโซเดียมไฮดรอกไซด์ (sodium hydroxide) หรือโพแทสเซียมไฮดรอกไซด์(potassium hydroxide) ประสิทธิภาพในการกำจัดโปรตีนด้วยด่างขึ้นกับอุณหภูมิในการทำปฎิกิริยา ความเข้มข้นของสารละลายด่างและอัตราส่วนระหว่างสารละลายด่างต่อปริมาณของเปลือกแข็ง โดยทั่วไปจะใช้สารละลายโซเดียมไฮดรอกไซด์เจือจางที่ความเข้มข้นตั้งแต่ 1-10% ในการทำปฎิกิริยากับเปลือกแข็งของสัตว์จำพวกกุ้งและปูที่อุณหภูมิสูง (65 -100 องศาเซลเซียส) นอกจากนี้ยังสามารถกำจัดโปรตีนจากเปลือกกุ้งและปูโดยการทำปฏิกิริยาที่อุณหภูมิ 90 องศาเซลเซียสและใช้อัตราส่วนของเปลือกต่อด่างเป็น 1:2 (w/v) โดยใช้สารละลายโพแทสเซียมไฮดรอกไซด์ที่ความเข้มข้นตั้งแต่ 1% หรือ 2% ตามลำดับ และปรกติใช้เวลาในการทำปฏิกิริยา 0.5 ถึง 6 ชั่วโมง การทำปฏิกิริยาในด่างเป็นเวลานานสามารถทำให้เกิดการสลายของสายพอลิเมอร์ (depolymerization) และหมู่แอซิติลถูกกำจัด อีกทางเลือกหนึ่งของวิธีการกำจัดโปรตีนคือ การใช้เอนไซม์ (enzymatic deproteinization) โปรตีนที่แยกด้วยวิธีการนี้จะมีคุณค่ามากกว่าในการนำไปใช้เป็นอาหารสัตว์หรือเป็นองค์ประกอบในอาหาร อย่างไรก็ตามการใช้เอนไซม์ไม่อาจรับรองได้ว่าจะสามารถกำจัดโปรตีนได้อย่างสมบูรณ์ เนื่องจากขึ้นอยู่กับประสิทธิภาพในการกำจัดโปรตีนของเอ็นไซม์และสภาวะในการทำปฏิกิริยา
C. กระบวนการกำจัดหรือฟอกสี (decolourization หรือ bleaching) สารสี (pigment) ในไคตินสามารถกำจัดได้โดยการสกัดด้วยอะซิโตน (acetone) คลอโรฟอร์ม (chloroform) เอธิลอะซิเตต (ethyl acetate) หรือ สารผสมระหว่างเอทานอลและอีเทอร์ (ethanol and ether mixture) และโดยปรกติทำการฟอกสีด้วยสารละลายโซเดียมไฮโปคลอไรท์ (NaOCl) หรือ ไฮโดรเจนเปอร์ออกไซด์ (H2O2)
2. การผลิตไคโตแซน โดยทั่วไปแล้วจะได้ไคโตแซนจากปฏิกิริยาการกำจัดหมู่แอซิติลของไคตินหรือที่เรียกว่า ปฏิกิริยา deacetylation ทำให้เอน-แอซิติลกลูโคซามีนซึ่งเป็นโมเลกุลเดี่ยวของไคตินถูกเปลี่ยนเป็นกลูโคซามีน ดังนั้นจากไคตินจึงเปลี่ยนเป็นไคโตแซน โดยทำปฏิกิริยากับสารละลายโซเดียมไฮดรอกไซด์ (sodium hydroxide) หรือโพแทสเซียมไฮดรอกไซด์ (potassium hydroxide) เข้มข้น (30-60% w/v) ที่อุณหภูมิตั้งแต่ 80-140 องศาเซลเซียส เป็นเวลานานถึง 10 ชั่วโมง แล้วแต่กรรมวิธีที่ใช้ อย่างไรก็ตามควรที่จะต้องควบคุมความเข้มข้นของสารละลายด่าง เวลาและอุณหภูมิในกระบวนการผลิตอย่างเคร่งครัดเนื่องจากมีอิทธิพลต่อระดับการกำจัดหมู่อะซิทิล น้ำหนักโมเลกุลและการจัดเรียงของหน่วยที่ถูกกำจัดหมู่แอซิติล (deacetylated unit) ในสายพอลิแซ็กคาไรด์ ซึ่งจากคุณสมบัติเหล่านี้ทำให้สามารถใช้ประโยชน์จากไคโตแซนได้มากมาย การเตรียมไคโตแซนโดยใช้โซเดียมไฮดรอกไซด์ที่ความเข้มข้นปานกลาง ณ อุณหภูมิค่อนข้างต่ำและใช้เวลานานทำให้เกิดการจัดเรียงของหน่วยที่ถูกกำจัดหมู่อะซิทิลอย่างไม่เจาะจงในโมเลกุลของไคโตแซนและช่วยลดการเกาะเป็นก้อน (aggregates) รวมทั้งการเกิดโครงสร้างอื่นๆ ส่วนการใช้อุณหภูมิสูงทำให้ระดับการกำจัดหมู่แอซิติลเพิ่มขึ้นแต่ก็ทำให้ขนาดโมเลกุลเล็กลงด้วย การทำปฏิกิริยากับด่างเป็นเวลานานไม่ทำให้การกำจัดหมู่อะซิทิลของไคตินเพิ่มขึ้นอย่างมีนัยสำคัญและไม่มีประโยชน์เนื่องจากทำให้สายพอลิเมอร์เกิดการแตกสลาย นอกจากนี้กระบวนการกำจัดโปรตีนก็มีผลต่อน้ำหนักโมเลกุลของไคโตแซนด้วยเช่นกัน และการมีออกซิเจนในระหว่างการทำปฏิกิริยาการกำจัดหมู่แอซิติลของไคติน จะมีผลต่อการแตกสลายของสายพอลิแซ็กคาไรด์จึงลดความหนืดและน้ำหนักโมเลกุลของผลิตภัณฑ์ที่ได้ลง
การเตรียมไคโตแซนที่มีระดับการกำจัดหมู่แอซิติลสูงกว่า 90% โดยไม่ให้เกิดการสลายตัวของโมเลกุลพอลิแซ็กคาไรด์นั้นเป็นสิ่งที่ทำได้ยาก แต่การลดระยะเวลาในการทำปฏิกิริยากับด่างลงโดยแยกกระบวนการกำจัดหมู่แอซิติลเป็นขั้นตอนย่อยๆจะช่วยให้น้ำหนักโมเลกุลของผลิตภัณฑ์เกิดการเปลี่ยนแปลงน้อยลง ซึ่งวิธีการหนึ่งที่สามารถกำจัดหมู่อะซิทิลได้เกือบสมบูรณ์คือการทำปฏิกิริยาของสารไคตินในสารละลายโซเดียมไฮดรอกไซด์ (ความเข้มข้น 50%) ที่อุณหภูมิ 4 องศาเซลเซียส เป็นเวลา 24 ชั่วโมงก่อน แล้วตามด้วยขั้นตอนการแยกและผสมกับสารละลายโซเดียมไฮดรอกไซด์ (ความเข้มข้น 10%) และให้ความร้อนสูงถึงอุณหภูมิ 230 องศาเซลเซียสและการลดความดัน (decompression) ของส่วนผสมลงอย่างรวดเร็ว
การผลิตไคโตแซนจากไคตินโดยใช้ด่างมักจะได้ผลิตภัณฑ์ที่มีน้ำหนักโมเลกุลและระดับการกำจัดหมู่แอซิติลที่แตกต่างและหลากหลาย ซึ่งการเปลี่ยนแปลงของระดับการกำจัดหมู่แอซิติลและน้ำหนักโมเลกุลที่เป็นผลมาจากสภาวะของกระบวนการผลิต ย่อมจะมีอิทธิพลต่อคุณสมบัติที่สำคัญในการนำไปใช้ประโยชน์ต่างๆ เช่น การละลายในกรด ความหนืดของสารละลายที่ได้ ตลอดจนฤทธิ์ทางชีวภาพ (biological activity) ของไคโตแซน จึงจำเป็นต้องพัฒนาวิธีการผลิตไคตินและไคโตแซนที่เป็นมาตรฐาน นอกจากนี้การใช้สารละลายด่างเข้มข้นจำนวนมากย่อมส่งผลกระทบต่อสิ่งแวดล้อม ดังนั้นอีกทางเลือกของผลิตไคโตแซนแทนวิธีการกำจัดหมู่อะซิทิลโดยการใช้ด่างคือ การแยกไคโตแซนที่เกิดขึ้นและมีอยู่แล้วตามธรรมชาติจากสิ่งมีชีวิตชั้นต่ำพวกเห็ดรา (fungal) หรือโดยการใช้เอนไซม์ chitin deacetylase
เส้นใยของพวกเห็ดราที่ผ่านการขจัดโปรตีนออกแล้ว สามารถนำมาสกัดไคโตแซนได้ด้วยกรดอะซิติกเจือจางและเติมสารละลายโซเดียมไฮดรอกไซด์เพื่อทำให้ตกตะกอน อีกวิธีหนึ่งคือการต้มเส้นใยของพวกเห็ดรากับสารละลายโซเดียมไฮดรอกไซด์เข้มข้น ซึ่งวิธีนี้สามารถกำจัดโปรตีนและลดหมู่แอซิติลของไคตินที่มีอยู่ในเซลล์ได้ด้วย จึงได้ปริมาณไคโตแซนเพิ่มขึ้นจากไคติน แต่อย่างไรก็ตามการใช้สารละลายด่างเข้มข้นทำให้เกิดการกำจัดหมู่แอซิติลและการสลายตัวของไคโตแซนอย่างมากเกินกว่าจะควบคุมได้ นอกจากนี้ผลผลิตไคโตแซนที่ได้จะมีการปนเปื้อนของสารกลูแคน (glucan) และไม่มีประโยชน์ต่อการนำไปใช้งาน ดังนั้นจึงควรเลือกใช้เห็ดราชนิดที่มีปริมาณไคโตแซนสูงเพื่อจะได้ตัดขั้นตอนการใช้ด่างในการกำจัดหมู่แอซิติลของไคติน
สำหรับการใช้เอนไซม์ไคตินดีอะเซทิเลสในการผลิตไคโตแซน หรือ โอลิโกเมอร์ของไคโตแซน (oligomers) ได้มีการศึกษาอย่างกว้างขวาง ถึงแม้ว่าไคติน (ซึ่งเป็นผลึกที่ไม่ละลายในน้ำ) จะต้านทาน (resistant) ต่อเอนไซม์ในการกำจัดหมู่แอซิติล แต่ไคตินที่ผ่านกระบวนทางเคมีเพื่อกำจัดหมู่แอซิติลไปบางส่วนแล้วสามารถนำไปกำจัดหมู่แอซิติลด้วยเอนไซม์ต่อไปได้ กระบวนทางเอนไซม์นี้จะมีประสิทธิภาพในกำจัดหมู่แอซิติลสำหรับโอลิโกเมอร์ของไคติน (oligomers) มากกว่า เพราะละลายน้ำได้และเข้าถึงเอนไซม์ได้ดีกว่า ปฏิกิริยาการลดหมู่แอซิติลด้วยเอนไซม์นี้จะได้โอลิโกเมอร์ของไคโตแซน (chitosan oligomers) ที่มีน้ำหนักโมเลกุลและปริมาณของ N-acetyl residues อยู่ในช่วงที่กำหนดได้แน่นอนซึ่งตรงข้ามกับการใช้กระบวนการทางเคมี ซึ่งสภาวะของวิธีการผลิตที่หลากหลายส่งผลให้ได้ไคโตแซนที่มีความแตกต่างกันในด้านต่างๆซึ่งได้แก่ระดับการกำจัดหมู่แอซิติล การกระจายตัวของหมู่แอซิติล ความยาวของสายพอลิเมอร์ โครงสร้างและน้ำหนักโมเลกุล ซึ่งสิ่งเหล่านี้จะมีอิทธิพลต่อการละลาย การยับยั้งการเจริญเติบโตของจุลินทรีย์ และคุณสมบัติอื่นๆ
